近日,中国农业科学院植物保护研究所作物有害生物功能基因组研究创新团队在国际著名学术期刊PLoS Pathogens上在线发表题为“CRISPR/FnCas12a-mediated efficient multiplex and iterative genome editing in bacterial plant pathogens without donor DNA templates”的研究论文。该研究借助异源表达的NHEJ修复系统,分别在水稻白叶枯病病原菌 Xoo PXO99A和番茄细菌性叶斑病病原菌 Pst DC3000中成功实现了CRISPR/FnCas12a核酸酶引起的基因组DNA双链断裂的高效修复,为植物病原细菌研究提供了新一代的遗传操作工具。
近些年来不断突破的CRISPR基因组编辑技术,因其精准、简单、高效等特性,极大促进了现代生命科学研究,已经广泛应用于真核生物中,如基因功能研究、人类疾病基因治疗、农作物新种质培育等。相比较而言,跟人类生活息息相关的原核生物的CRISPR研究远远滞后。在大多数农作物重要病原细菌中,CRISPR系统具有细胞毒性,严重制约其应用。
在该研究中,研究人员利用来源于新弗朗西斯菌 Francisella novicida 的CRISPR/FnCas12a系统(CRISPR-Solo策略),实现了 Xoo PXO99A的外源质粒高效去除。结合使用来源于结核分枝杆菌 Mycobacterium tuberculosis 的非同源末端连接(NHEJ)途径的LigD和Ku蛋白(CRISPR-NHEJ策略),在 Xoo PXO99A基因组中成功实现了高效单基因、多基因编辑,以及基因簇片段删除。进一步使用迭代策略,靶向编辑PXO99A中Non-TAL效应蛋白编码基因家族,成功创制出25个non-TAL基因突变的编辑菌株PXO99AD25E。进一步全基因组测序表明,CRISPR/FnCas9系统在 Xoo 中未引起明显的脱靶效应。另外,该研究表明CRISPR Solo和CRISPR-NHEJ策略也适用于 Pst DC3000中内源质粒消除和基因组靶基因编辑。CRISPR-Solo和CRISPR-NHEJ策略,为植物病原细菌基因功能研究提供了一系列解决方案,也为后续高效便利的PXO99A全基因组打靶操作、工程菌株开发等奠定了重要基础。
中国农科院植保所为该论文的第一完成单位,严芳副研究员、王敬文和张素杰硕士生为论文共同第一作者,周焕斌研究员为论文通讯作者。此外,植保所周雪平教授、冯洁研究员和徐进副研究员、南京农业大学宋从凤教授、上海交通大学陈功友教授、中国农科院作科所纪志远副研究员等也参与了此项工作。该研究得到中央级公益性科研院所基本科研业务费专项和中国农业科学院农业科技创新工程专项资金的资助。
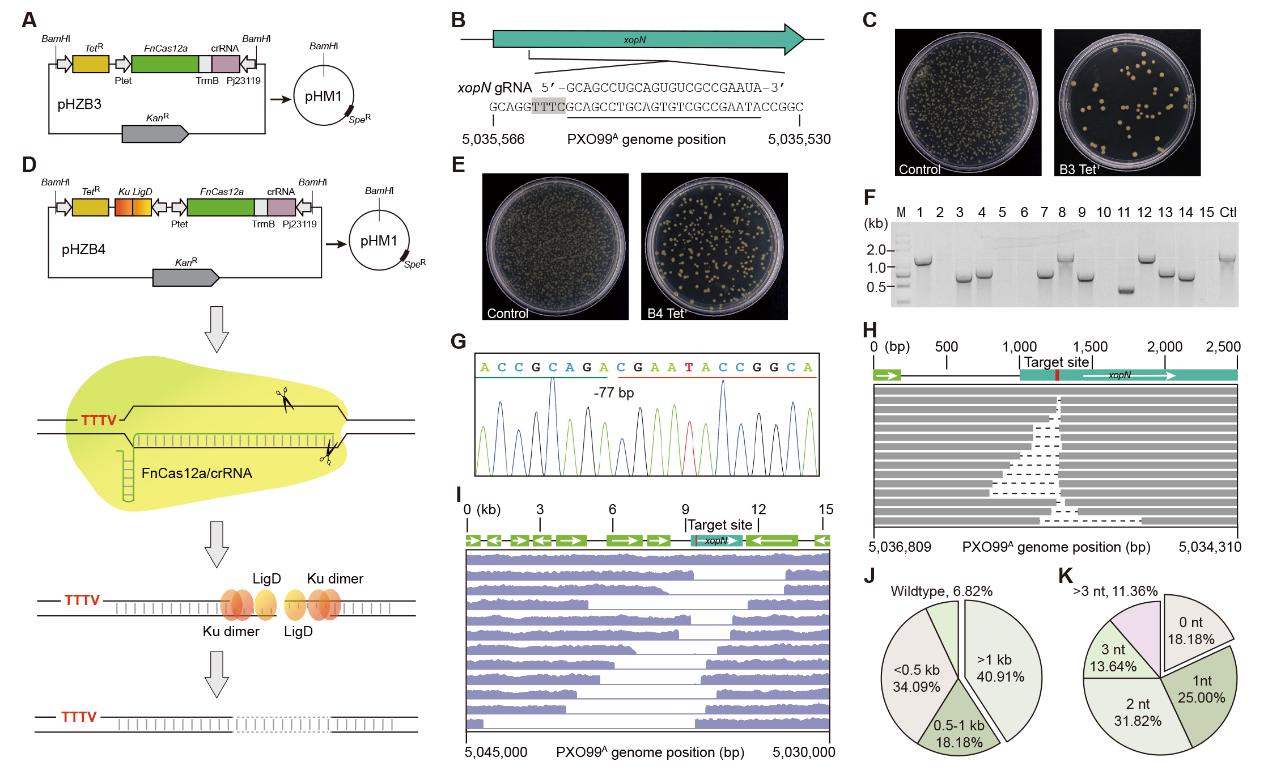
Xoo PXO99A基因组编辑技术
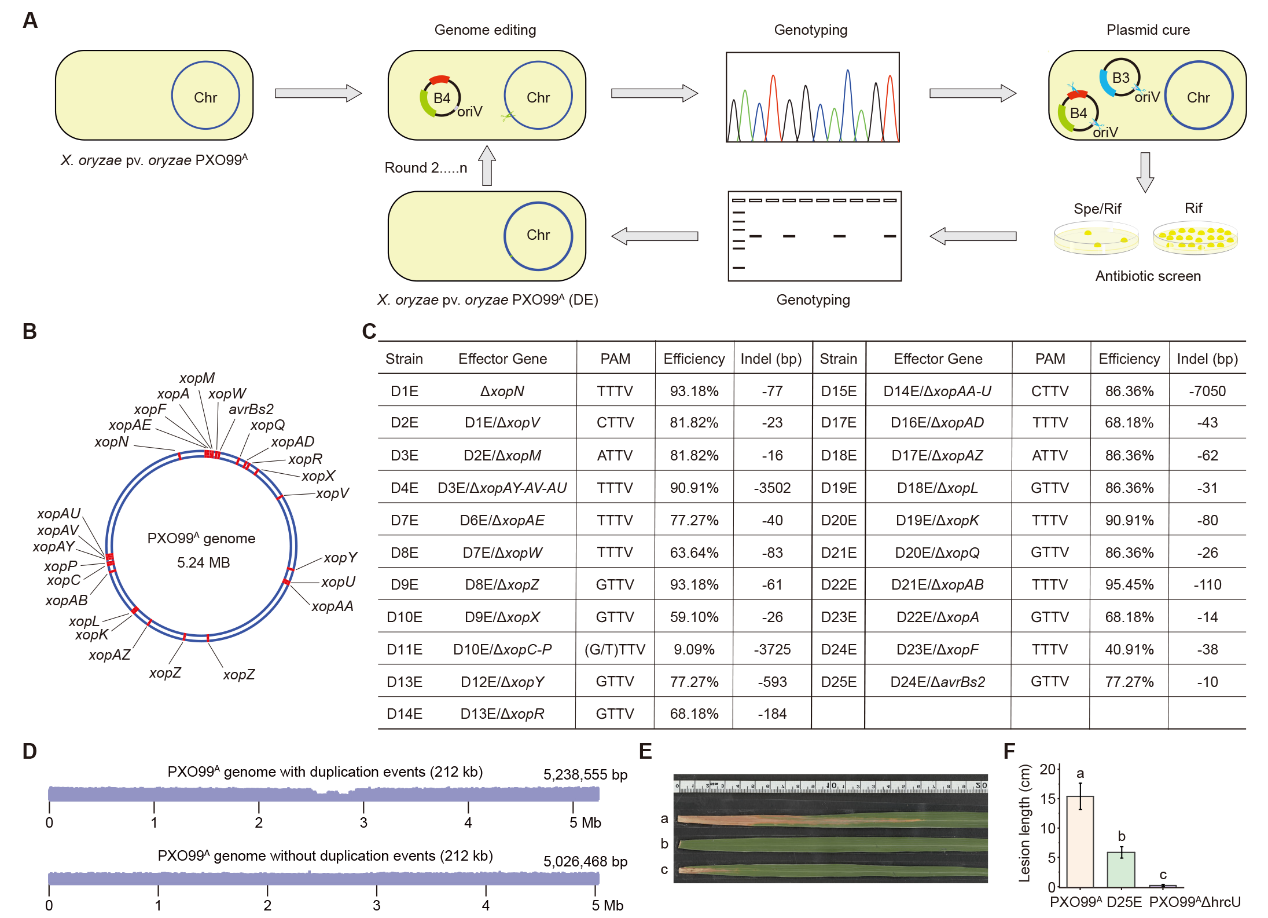
迭代基因组编辑创制PXO99AD25E突变体
原文链接:https://doi.org/10.1371/journal.ppat.1010961